Celebriamo 30 anni di innovazioni ottenute grazie alla Bioluminescenza
Luciferasi: dalla natura al laboratorio
La coda splendente di una lucciola o le onde blu dell'oceano sono un piccolo assaggio della presenza della bioluminescenza in natura. Fin dai primi anni della ricerca biochimica e della biologia molecolare, questo fenomeno naturale è stato identificato dai ricercatori come un potente strumento per lo sviluppo di saggi biologici. Nel 1991 Promega ha messo sul mercato i primi prodotti basati sulla luciferasi, dando il via ad uno sviluppo continuo di soluzioni che ora include un vastissimo assortimento di prodotti, tutti fondati sulla bioluminescenza e le continue innovazioni da essa derivate. In questa pagina illustreremo nel dettaglio come nel corso degli anni e grazie agli incredibili progressi scientifici compiuti dal nostro R&D, Promega sia riuscita a sprigionare il pieno potenziale di questa risorsa naturale, mettendolo a disposizione dei ricercatori di tutto il mondo.


Research and Product Spotlight
NanoBiT® Technology
NanoLuc® Luciferase has been engineered into a complementation reporter system termed “NanoLuc Binary Technology" or NanoBiT. The NanoBiT® system consists of an optimized large subunit from NanoLuc, LgBiT, along with small 11-amino-acid subunits that have variable affinity for the LgBiT subunit. Structural complementation of both subunits reconstitutes a bright luciferase enzyme.
NanoBiT® technology creates new possibilities for using bioluminescence to study protein dynamics. Using the low affinity small subunit, SmBiT, sensitive live-cell protein:protein interaction assays can be created by fusing LgBiT and SmBiT to target proteins of interest. In contrast the high affinity small subunit, HiBiT, self-associates with the LgBiT peptide, making HiBiT an easily detected and highly sensitive protein tag. The HiBiT protein tagging system can be used for both intracellular and extracellular protein detection, and when combined with CRISPR-based tagging, allows creation of knock-in reporter models that accurately reflect endogenous protein biology. Most recently NanoBiT has been further adapted into Lumit™ Technology for detection of specific antigens or antibodies, bringing the power of bioluminescence to immunoassay applications.
NanoBRET™ Technology
The small size and bright light output from NanoLuc are ideal characteristics for use as a protein tag. Together with a narrow, blue-shifted emission spectrum, these qualities make NanoLuc an ideal energy donor in Bioluminescence Resonance Energy Transfer (BRET) applications. Combined with red-shifted energy-accepting fluorophores, the NanoBRET™ system has optimal spectral overlap, increased signal and lower background compared to conventional BRET assays.
These fluorophores can be added to molecules such as protein ligands to create NanoBRET™ Target Engagement assays for measuring small molecule binding to target proteins or configured as HaloTag® ligands for monitoring protein:protein interactions in live cells using Nanoluc® and HaloTag® fusion proteins. Live-cell substrate options allow for a stable NanoLuc donor signal that can last for hours to days, enabling new opportunities for understanding protein dynamics within the cellular environment.

Watch how researchers from Keele University have used a NanoBiT® PPI assay to screen for novel autophagy inhibitors.

Watch how Aurelia Bioscience is using NanoBRET™ Target Engagement to screen Kinase-binding compounds in live cells.

NanoLuc® Luciferase
Oltre ad utilizzare la firefly luciferase per la quantificazione di ATP o per il suo canonico scopo di gene reporter, è anche possibile utilizzarla per quantificare variazioni nel quantitativo del suo substrato: la luciferina. Accoppiando la reazione con dei pro-substrati modificati dall’aggiunta di porzioni specifiche e selettive per determinate classi enzimatiche è stato possibile creare sistemi “add-mix-measue” per misurare l’attività di diverse proteasi ed enzimi metabolici, sfruttando il fatto che la quantità di pro-substrato convertito sia proporzionale all’attività dell’enzima che lo converte. Il sistema Caspase-Glo® 3/7 è uno dei primi esempi in cui la tecnologia è stata utilizzata in questo modo, permettendo di ottenere un saggio sensibile e specifico per la quantificazione delle cellule che entrano in apoptosi. Questa tipologia di saggi, per le consuete caratteristiche di sensibilità, riproducibilità e alto throughput, si presta all’utilizzo in drug discovery, offrendo alla comunità scientifica e alle industrie farmaceutiche un tool impareggiabile per lo sviluppo di nuovi farmaci, soprattutto in ambito oncologico. Questo stesso sistema è stato recentemente ottimizzato anche per l’utilizzo in colture cellulari 3D, permettendone l’utilizzo in sistemi più vicini alle reali condizioni fisiologiche.
Learn more about measuring apoptosis in 3D culture systems ›

In addition to using the firefly luciferase reaction to measure the amount of luciferase or ATP in a sample, it is also possible to measure changes in substrate (luciferin) concentration. By coupling the reaction with pro-luciferin substrates containing protecting groups that can be reacted upon by different enzyme classes, sensitive add-and-read assays have been created to measure the activity of various proteases and metabolizing enzymes, where the amount of light produced is proportional to enzyme activity. The Caspase-Glo® 3/7 Assay System was an early example of this approach, allowing for a simple, sensitive method to detect cells undergoing apoptosis. The ability to easily measure apoptotic cell death has allowed oncology researchers to efficiently screen for and characterize potential therapeutic approaches that can lead to the removal of cancer cells. Recently, this approach has been further adapted to enable the measurement of apoptosis in 3D culture systems, allowing scientists to study induction of apoptosis in model systems that more accurately mimic tumor cell growth.
Learn more about measuring apoptosis in 3D culture systems ›
Il Dual-Luciferase® Reporter Assay System (DLR) è stato il primo reagente capace di integrare la Firefly luciferasi e Renilla come co-reporter, consentendo il rilevamento sequenziale di due reporter dallo stesso campione. A differenza di altre opzioni a doppio reporter, il dosaggio DLR ™ ha fornito ai ricercatori un metodo di normalizzazione interna semplice e in grado di offrire velocità, sensibilità e linearità di segnale sia per i reporter sperimentali che per quelli di controllo. Il sistema DLR ™ inoltre, ha offerto miglioramenti significativi nella gestione sperimentale; entrambi i reporter infatti potevano essere rilevati dallo stesso campione semplicemente aggiungendo in sequenza i due reagenti grazie all’innovativa chimica "Stop & Glo", eliminando così la necessità di dividere i lisati e rilevare i due reporter separatamente.
Il sistema DLR ™ è stato utilizzato negli ultimi 20 anni per aiutare i ricercatori a far progredire la nostra comprensione degli elementi genomici che regolano l'espressione genica e lo ritroviamo in larga parte degli studi su regolatori trascrizionali come Hif1A (risposta all'ipossia) e NF-kB (infiammazione e risposta immunitaria). Il concetto dual-luciferase® si è ulteriormente evoluto arrivando alle nuove versioni Dual-Glo® Luciferase Assay System, basata su una versione stabilizzata dei reporter che permette l’utilizzo con alti throughput senza necessità di iniezione, e il Nano-Glo® Dual-Luciferase® Reporter Assay System, che consente di utilizzare NanoLuc e Firefly come co -reporter. Inoltre, il dosaggio DLR ™ continua oggi ad essere utilizzato in campi che vanno dallo sviluppo di farmaci alla produzione di colture e fino alla virologia. Guarda come gli scienziati stanno applicando il dosaggio DLR™ ›

Scopri come il premio Nobel Gregg L. Semenza ha usato il dual-reporter assays per migliorare la comprensione dell’ipossia.
Leggi di più sul lavoro di SemenzaIl Luciferase Assay System (LAR) è stato il primo reagente basato sulla luciferasi lanciato da Promega, nel 1991 insieme al gene reporter luc per la firefly luciferase. Ancora oggi il sistema LAR è uno dei più performanti, basato su una chimica di tipo flash che ne richiede l’utilizzo in associazione ad un iniezione automatizzata. Negli ultimi 30 anni LAR è stato utilizzato in migliaia di progetti di ricerca, permettendo di rispondere a tantissimi quesiti sulla regolazione dell'espressione genica o sull'analisi funzionale dei polimorfismi. Trent’anni dopo, il LAR è ancora uno strumeno prezioso per lo sviluppo dei vaccini e dei trattamenti terapeutici per infezioni da SARS-CoV-2.
I primi vettori reporter (pGL2) della lucciola luciferasi (Fluc) disponibili in commercio hanno utilizzato il gene luciferasi della lucciola nativo, luc, come reporter. Tuttavia, è apparso chiaro come un'ulteriore ingegneria genetica potrebbe migliorare le prestazioni di questo sistema reporter. La successiva generazione di reporter FLuc (pGL3) ha infatti introdotto un nuovo gene, luc+, con ottimizzazione del codone dei mammiferi per una migliore espressione del reporter e un miglioramento alla spina dorsale del vettore per ridurre l'espressione di fondo. Questi passaggi di ingegneria hanno aumentato l'attività della luciferasi da 20 a 100 volte rispetto a quanto si poteva ottenere con il sistema pGL2. Questo aumento nelle prestazioni è stato ulteriormente migliorato con la serie di vettori pGL4 che ha introdotto il gene reporter luc2. Tra i progressi, un'ulteriore ottimizzazione dei codoni, la rimozione di sequenze regolatorie criptiche e l'introduzione di geni luciferasi destabilizzati per migliorare i tassi di risposta. Il design pGL4 ha saputo creare un sistema reporter capace di esprimersi in modo uniforme e ottimale nelle cellule ospiti dei mammiferi, riducendo al minimo le risposte fuori bersaglio e rispondendo rapidamente alle dinamiche trascrizionali.
Quando la luciferasi interviene nello sviluppo di trattamenti anti malaria
Scopri come è stata sfruttato il potere della luciferasiFirst generation luciferase detection assays have very bright but short-lived signal and require lysate generation prior to addition of assay reagents. Although extremely powerful, the short signal duration and upstream processing requirements present challenges to researchers using bioluminescent reporters in high-throughput analysis. The second generation “Glow” reagents such as the Bright-Glo™ and Steady-Glo® Assay Systems overcame these limitations by extending the kinetics of the firefly luciferase reaction (30 minute and 5-hour respective half-lives) while also providing a single-addition reagent that is added directly to cells in culture to lyse the cell and provide all of the assay components. These “add-mix-measure” assays significantly simplified sample processing and brought compatibility to microplate workflows allowing researchers to batch process 10s to 100s of plates at a time, expanding the use of luciferase reporter assays to high-throughput screening applications.
Learn more about the differences between Flash and Glow assays ›
ATP is well recognized as an indicator of metabolically active cells, making the measurement of total ATP levels an important tool in determining the impact of compound treatment on cell viability. The CellTiter-Glo® Luminescent Cell Viability Assay uses the cell as source of the ATP in the luciferase reaction, producing a bioluminescent signal that is proportional to the number of viable cells in a well. Similar to other “Glow”-type luciferase assays, the luminescent signal has an extended half-life ( > 5hr), and the reagent can be added directly to cells in culture making it ideal for automated high-throughput cell proliferation and cytotoxicity assays. The assay has been further optimized to reduce preparation time and simplify repeat use in the CellTiter-Glo® 2.0 assay and has also been adapted to measuring cellular ATP in 3D model systems for determining cell viability in these more complex physiological models.
Guarda come la Dr. Samantha Llewellyn usa CellTiter-Glo® 3D per valutare la tossicità in modelli epatici 3D più fisiologicamente rilevanti rispetto alle colture monostrato standard.
Una Glo-riosa storia di innovazione e scoperta
Ripercorriamo 30 anni di scoperte pionieristiche ed innovazione legati alla bioluminescenza


Luciferase Assay System
Nasce il primo reagente per la quantificazione della luciferasi prodotto da Promega, che permette lo studio dell’espressione genica senza ricorrere al radioattivo. Ancora oggi il sistema LAR assay è uno dei più performanti, basato su una chimica di tipo flash che ne richiede l’utilizzo in associazione ad un iniezione automatizzata. Il LAR, insieme al gene reporter per la firefly luciferase (luc), è stato uno dei primi strumenti a permettere la mappatura dei meccanismi di regolazione genica.
Scopri tutti i nostri geni reporter bioluminescenti
Dual-Luciferase® Reporter Assay System (DLR)
DLR è stato il primo reagente a permettere il rilevamento sequenziale di un secondo reporter in un singolo campione. DLR ha rivoluzionato il mondo dei sistemi reporter, consentendo una normalizzazione interna dell'attività della luciferasi fondamentale per l’analisi e la riproducibilità dei dati.
Scopri gli utilizzi del sistema Dual-LuciferaseVettori Reporter pGL
La famiglia di vettori reporter pGL3 presenta un gene modificato della firefly luciferase, luc +. Il processo di perfezionamento del gene reporter è poi continuato fino ad arrivare ai reporter pGL4 e luc2, tramite analisi bioinformatiche.
pGL4 Luciferase Reporter Vectors Tool
ENLITEN®/UltraGlo™ Recombinant Luciferase
Promega aveva già prodotto una firefly luciferase ricombinante (Enliten) in precedenza, ma questa è stata ottimizzata fino a creare una luciferasi termostabile, chiamata UltraGlo. Lo sviluppo di UltraGlo è stato fondamentale per realizzare saggi più stabili e robusti, che permettessero di passare ad un approccio semplificato di tipo «add&read».
ENLITEN® ATP Assay SystemBright-Glo™ (1999), Steady-Glo® (1998), Dual-Glo® (2001) Luciferase Assay Systems
Il continuo sviluppo e miglioramento delle cinetiche correlate alle tecnologie bioluminescenti ha portato alla nascita di Bright-Glo, Steady-Glo e Dual-Glo, permettendo finalmente l’utilizzo del sistema in piastre multi pozzetto. Il formato «add&read» semplifica il protocollo e consente di ampliare al massimo la processività, rendendolo un sistema high througput.
Find the Best Reporter AssayCellTiter-Glo® Cell Viability Assay
Con lo sviluppo della luciferasi UltraGlo èstato possibile creare un sistema «add&read» per la quantificazione dell’ATP, che si è rivelato essere un biomarker cruciale per la vitalità cellilare. Così nasce CellTiter-Glo , che diventa il gold standard per la quantificazione della vitalità cellulare, anche grazie alla compatibilità con sistemi high-througput. Il principio chimico del saggio ha consentito lo sviluppo di altre tecnologie che misurano l'ATP, in particolare i saggi enzimatici Kinase-Glo (2004) e ADP-Glo(2009), utilizzati per studiare enzimi ATPasi come le chinasi.
Scopri gli utilizzi di CellTiter-Glo in ambito COVID-19
Caspase-Glo® 3/7 Assay
Oltre a quantificare la luciferasi o l’ATP in un campione utilizzando la chemiluminescenza, il passo successivo è stato misurare il consumo del substrato (luciferina). Accoppiando la luciferina con gruppi protettivi specifici per diverse classi di enzimi, si possono ottenere saggi «add&read» ultra sensibili quantificare l’attività di questi ultimi. Nascono così i sistemi per la quantificazione dell’attività delle caspasi, fondamentali per lo studio dei meccanismi apoptotici.
Caspase-Glo® Assay nella ricerca contro il cancro Explore Caspase-Glo®
ONE-Glo™ Luciferase Assay System
Una maggiore comprensione della chimica di reazione della firefly luciferasi, oltre all’arrivo in Promega di un vero e proprio team di biologi e chimici dedicati a questi prodotti, permette la creazione di una luciferina migliorata. Questo nuovo substrato, la fluoroluciferina, è un primo esempio di sviluppo di un nuovo substrato per la chemiluminescenza.
Pseudovirus e Luciferasi Discover ONE-Glo™
NanoLuc® Luciferase
L'esperienza nello sviluppo della chimica della bioluminescenza sfocia nella progettazione di un nuovo reporter. Nata da una luciferasi di gamberetto, la nuova luciferasi NanoLuc è sviluppata per essere un piccolo monomero (19kDa) che utilizza un substrato unico, offrendo una sensibilità di circa 100 volte superiore rispetto ai sistemi firefly o Renilla. Questo nuovo reporter viene utilizzato in molte applicazioni e servirà come punto di partenza per la nascita di nuove tecnologie reporter.
pri come i ricercatori usano la NanoLuc Luciferasi per creare modelli di disturbi cardiovascolari
NanoBRET™ Technology
Gli sforzi per lo sviluppo di NanoLuc portano alla nascita di una vera e propria piattaforma per numerose tecnologie. Le dimensioni ridotte e la potenza luminosa di NanoLuc infatti offrano caratteristiche uniche ed ideali per la marcatura proteica e ne permettono l’utilizzo come donatore di energia in sistemi BRET. E’ stato quindi sufficiente identificare un fluoroforo dallo spettro compatibile per costituire il sistema NanoBRET, ideale non solo per lo studio in cellule vitali dell’interazione tra proteine, ma anche per la quantificazione dell’interazione e del tempo di occupazione che le molecole hanno con recettori o proteine bersaglio.
Leggi come usare NanoBRET per studiare il Kinome
NanoBiT® Technology
In virtù delle grandi ed uniche qualità di Nanoluc, In Promega si inizia a pensare di usarla per un sistema a multi-subunità. Questa tecnologia, denominata "NanoLuc Binary Technology" o NanoBiT, consiste nella suddivisione dell’enzima nativo in due subunità: un piccolo tag di 11 aminoacidi e una porzione più grande e globulare chiamata LgBiT. La complementazione delle due parti ricostituisce un enzima brillante e funzionale che può essere usato per la quantificazione. Ottimizzando l’affinità del peptide da 11 aa è stato possibile creare SmBiT, un peptide a bassissima affinità da utilizzare in studi di interazione tra proteine, e HiBiT, un tag ad altissima affinità che permette di marcare le proteine per una quantificazione super efficiente. L’estrema sensibilità del sistema e le ridotte dimensioni di HiBiT permettono l’utilizzo di questo metodo per la marcatura di target endogeni tramite meccanismi di genome editing come il CRISPR.
Come si adatta NanoBiT a saggi biochimici?
Lumit™ Technology
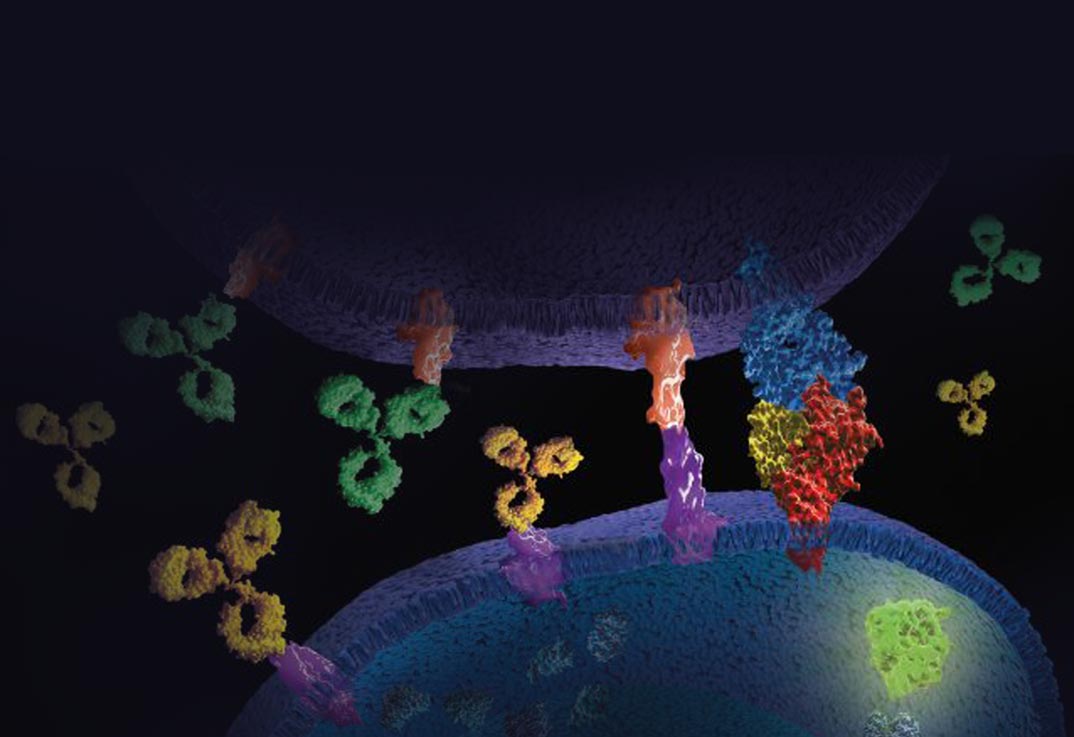
In seguito allo sviluppo della tecnologia NanoBiT, viene riconosciuto come questo sistema potrebbe essere utilizzato per rilevare un'ampia varietà di analiti attraverso la coniugazione delle sue subunità ad anticorpi usati per i comuni saggi immunologici. La tecnologia risultante, ora chiamata Lumit, permette analisi immunologiche quantitative semplici, robuste e ad alta sensibilità.
Scopri la tecnologia Lumit™
Coming Soon: Bioluminescence Applications Guide
Vuoi saperne di più sui vantaggi dei reporter genetici bioluminescenti e su come questi possono essere applicati alla tua ricerca? Scarica l’anteprima del capitolo 2 «Reporter e saggi genetici bioluminescenti» dalla nostra Guida alle applicazioni di bioluminescenza.

Presente e passato si incontrano
Il Turner TD-20/20 è stato uno dei primi luminometri a offrire i doppi iniettori e questa peculiarità lo ha reso uno strumento perfetto per eseguire il dosaggio Dual-Luciferase.
Se vuoi saperne di più, ci sono tante cose sorprendenti che puoi scoprire sullo strumento che fin dal principio ha permesso di sfruttare i reagenti Promega…
La soluzione integrata per le migliori performance


Le migliori soluzioni sul mercato per ottenere il massimo da tutti i sistemi bioluminescenti