Articoli correlati
Luciferasi NanoLuc®: il futuro luminoso dell'imaging in vivo ›
Notice: Promega will be performing essential system updates January 21–25.
Order processing and shipping will pause starting January 21 at 4:00 PM CST and resume on January 26.
Please plan to order in advance for any products needed during this timeframe.
Please contact Customer Service with any questions.
Grazie per aver verificato il tuo indirizzo email.
C'è stato un errore nella verifica dell'indirizzo email. Riprova o contatta il servizio clienti
11.04.22 – Giacomo Grisafi

I PROTAC potranno non essere l'argomento di conversazione durante un cocktail party, ne meritare la copertina di riviste glamour, ma stanno sicuramente scuotendo l'industria della drug discovery grazie alla loro capacità di superare i limiti della farmacologia tradizionale, permettendo di fatto il "drug the undrugable".
In questo articolo blog proviamo a fornire una panoramica sui PROTAC, rispondendo alle domande più frequenti su questo argomento.
L'acronimo PROTAC sta per "proteolysis targeting chimera". Sono molecole contenenti più unità funzionali che vengono utilizzate per indirizzare proteine specifiche verso la degradazione, tramite il sistema di smaltimento dei rifiuti cellulari (il sistema ubiquitina-proteasoma o UPS). Un PROTAC solitamente è costituito da due unità funzionali responsabili del legame selettivo, separati da un linker.
La natura bifunzionale di un PROTAC è fondamentale per il suo funzionamento all'interno della cellula. La prima unità funzionale si lega in maniera selettiva alla proteina di interesse (target) mentre l'altra ne guida l'interazione con l'UPS, solitamente tramite interazione con la E3 ligasi. Il legame simultaneo di queste due proteine da parte del PROTAC determina la formazione di un complesso ternario. Una volta formato questo complesso, la E3 ligasi catalizza l'aggiunta sequenziale di residui di ubiquitina alla proteina bersaglio, formando una catena di ubiquitina che attiva l'UPS, portando alla degradazione della proteina bersaglio.
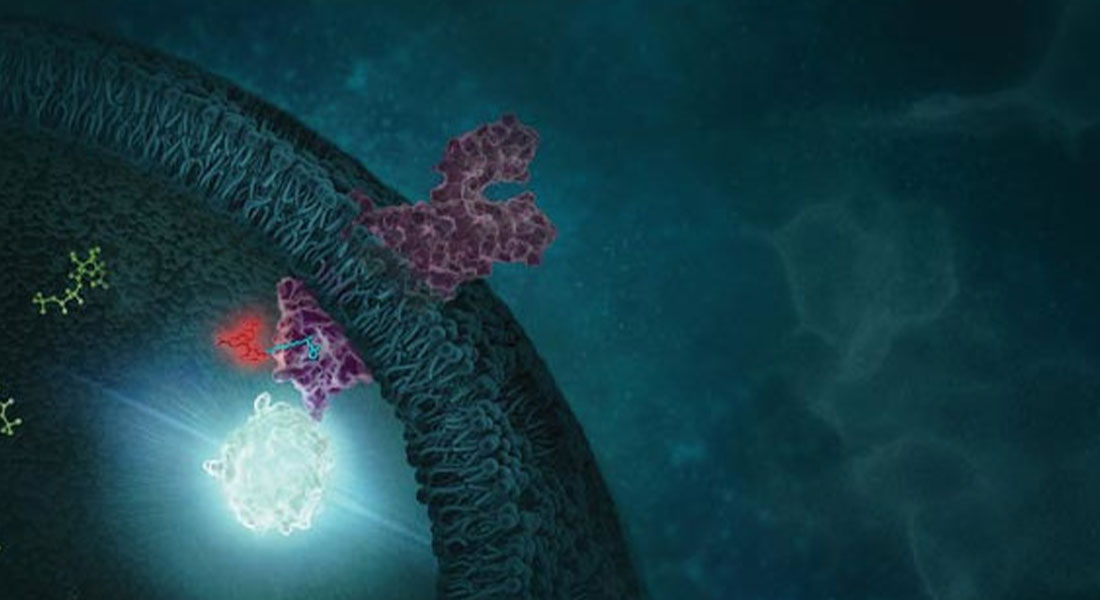
È importante notare come il PROTAC venga rilasciato dopo l'ubiquitinazione della proteina bersaglio, tornando quindi disponibile nell'ambiente cellulare per il legame e la degradazione di ulteriori molecole di proteina target. Pertanto, una quantità relativamente piccola di PROTAC può catalizzare la degradazione di una grande quantità di proteina bersaglio.
Una volta che una proteina bersaglio è stata identificata come associata a una malattia, le tradizionali strategie di drug discovery si concentrano sulla ricerca di inibitori per quella proteina, in modo da inattivarla. In molti casi, questo approccio prevede lo screening di un vasto numero di small molecules candidate. Un approccio farmacologico con dei limiti (1), specialmente per le proteine che non hanno attività enzimatica. Di conseguenza, si stima che l'85% dei bersagli proteici noti rimanga "undruggable" proprio perché manca di un sito di legame attivo da bloccare (2). Inoltre, anche nei casi in cui esistano inibitori adeguati, sono spesso necessarie alte concentrazioni di questi farmaci per ottenere effetti terapeutici rilevanti(3).
I PROTAC vanno oltre questi limiti perché possono essere progettati in modo da legare anche porzioni non funzionali della proteina target. Inoltre, specialmente quando si studiano vie di segnalazione complesse, la degradazione di una proteina bersaglio può offrire un vantaggio rispetto alla semplice inibizione della sua attività.
Il primo PROTAC scoperto è stato un peptide sintetizzato e testato dai laboratori di Craig Crews e Raymond Deshaies nel 2001 (4). In questo studio proof-of-concept, il PROTAC è stato progettato per indirizzare l'enzima metionina aminopeptidasi-2 (MetAP-2) a un componente del complesso dell'ubiquitina ligasi. Lo studio ha mostrato come Met-AP2 sia stato ubiquitinato e degradato in modo dipendente da PROTAC, ponendo le basi per il futuro sviluppo del modello PROTAC vero e prorio. A questo primo studio sono seguite altre applicazioni di PROTAC a base di peptidi, ma si è trattato di molecole spesso rese inefficaci a causa della loro scarsa permeabilità cellulare (5).

La prima vera applicazione di successo di PROTAC è stata pubblicata nel 2008 (6), con una molecola che ha mostrato una buona permeabilità cellulare associata ad una buona efficienza di degradazione per il recettore degli androgeni. Un risultato che ha suggerito applicazioni per curare un cancro alla prostata caratterizzato da una maggiore espressione proprio del recettore in esame.
Da queste prime scoperte la ricerca PROTAC ha registrato una crescita tanto esponenziale (7) che ad oggi lo sviluppo di PROTAC offre un'interessante alternativa per la drug discovery al tradizionale approccio basato su inibitori.
Sono molteplici i fattori da considerare nella progettazione di un PROTAC. Sebbene gli studi strutturali possano fornire, a partire dai dati cristallografici, informazioni sul sito di legame per i target di interesse, questi dati non sono disponibili per molti target o potenziali PROTAC. Di conseguenza, la progettazione di PROTAC è guidata dall'esame degli aspetti meccanicistici di ciascuna fase del processo di degradazione proteica mirata. Considerazioni generali per la progettazione PROTAC sono state pubblicate da Paiva e Crews (8), mentre Leissing et al. hanno presentato una panoramica dei principi di progettazione guidata dalla struttura, con un'enfasi sulla formazione di complessi ternari (9). Uno terzo articolo ha invece discusso la progettazione del PROTAC per colpire componenti complessi di rimodellamento della cromatina implicati in diversi tipi di cancro (10).
Tipicamente, la progettazione di PROTAC si concentra su ogni componente della molecola: la componente che lega il bersaglio, il linker e il sito di legame e recrutamento della E3 ligasi.
E' necessario che ciascun PROTAC abbia una componente altamente selettiva per il legame alla proteina bersaglio. Sebbene non sia necessario utilizzare molecole inibitrici per sviluppare un PROTAC, i vantaggi della rimozione della proteina rispetto alla sua inibizione permettono di partire da comuni inibitori e potenziarne l'effetto. Tuttavia, anche molecole con scarsa affinità per la proteina target possono essere stabilizzate per la formazione di complessi ternari, portando a un'efficiente degradazione proteica mirata (11).
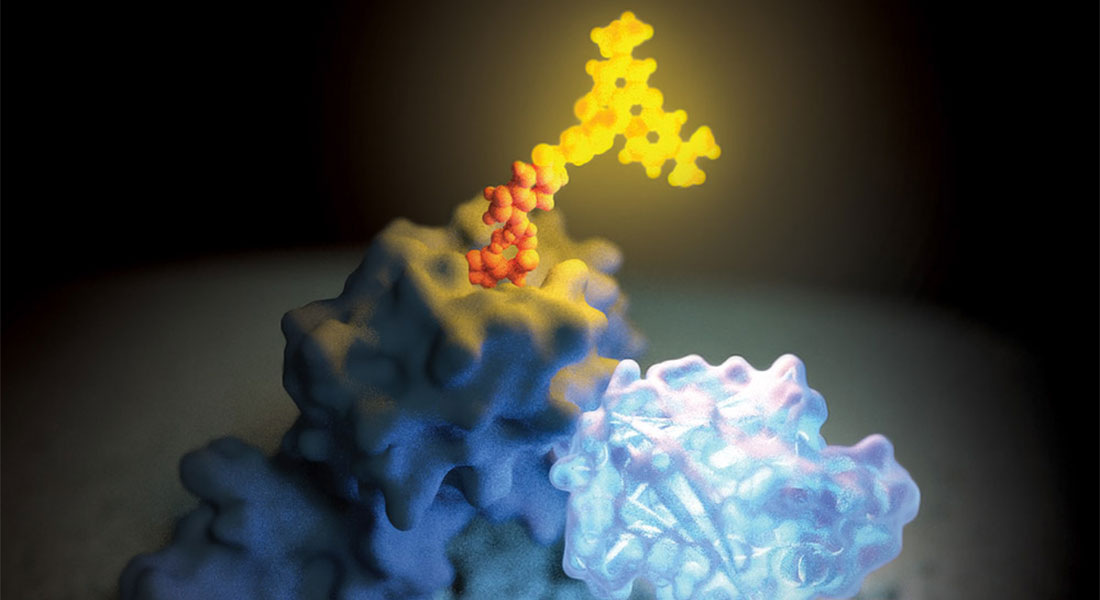
Una scoperta interessante nello sviluppo di PROTAC è l'uso di PROTAC trivalenti (12). Queste molecole includono due siti di legame per la proteina bersaglio, portando a una maggiore stabilizzazione del complesso ternario e, di conseguenza, una migliore degradazione.
L'importanza del linker PROTAC viene spesso sottovalutata in fase di progettazione, ma anche il linker può avere un ruolo nell'efficacia dell'azione del PROTAC in cui è inserito. La preferenza è quindi verso l'utilizzo di linker più complessi e funzionali, con vantaggi nella stabilizzazione del complesso ternario e miglioramenti complessivi nell'efficienza della degradazione (13). Sia la composizione del linker che la lunghezza dello stesso svolgono un ruolo importante nell'ottimizzare l'efficienza del PROTAC (14).
Ad oggi sono conosciute più di 600 E3 ligasi; tuttavia, la maggior parte dello sviluppo di queste porzioni del PROTAC è diretto a una piccola quantità di questi enzimi (15). Tra questi, i più comuni sono la von Hippel-Lindau (VHL) E3 ligasi e cereblon (CRBN). Esiste una pubblicazione che fornisce informazioni sui percorsi sintetici disponibili durante la progettazione di queste subunità PROTAC (15); un articolo che comprende anche uno strumento che facilita la selezione di un ligando adatto, nonché un elenco di elementi costitutivi disponibili in commercio per lo sviluppo di ligandi per E3 ligasi.
Esiste una gran varietà di test biochimici per esaminare ogni fase del processo di degradazione proteica mirato; tuttavia, i metodi tradizionali in genere forniscono risultati end point e non sono adatti per analisi HTS. Al contrario, i test su cellule vive per monitorare la degradazione in tempo reale offrono vantaggi significativi (16). Di questi test, i metodi basati su NanoBRET™ offrono una misurazione sensibile e conveniente della cinetica del PROTAC, nonché una più ampia comprensione dei complessi processi di degradazione all'interno di un contesto complesso e dinamico come quello intracellulare (17). Gli Starter Kit NanoBRET™ VHL e CRBN per complessi ternari forniscono un metodo efficiente e affidabile per misurare la formazione di complessi ternari e, contemporaneamente, quantificare la degradazione delle proteine bersaglio.
Il primo PROTAC ad entrare in studi clinici, nel 2019, è stato sviluppato da Arvinas Inc. per il trattamento del cancro alla prostata. Nel febbraio 2022 invece, la stessa società ha riportato risultati preliminari in cui si affermava che la strategia PROTAC "continua a fornire prove dell'attività antitumorale e del beneficio per il paziente nel carcinoma prostatico metastatico resistente alla castrazione (mCRPC)". In collaborazione con Pfizer, Arvinas ha anche riportato risultati iniziali incoraggianti per un altro PROTAC, ARV-471, nel trattamento del cancro al seno, mentre l'ipotesi di approccio tramite PROTAC si estende ormai a molti altri tipi di cancro ( 18, 19). Uno sviluppo promettente negli studi preclinici è l'uso dei PROTAC per colpire i tumori guidati da KRAS, storicamente difficili da aggredire e trattare in modo efficace (20).
Vorresti lavorare con i PROTAC ma non sai da dove iniziare? Scopri tutte le nostre soluzioni.
Riferimenti
Ti è piaciuto il nostro articolo? Condividilo!