Contenuti Correlati
Entra nella galassia Promega con GloMax® Galaxy Bioluminescence Imager ›
Notice: Promega will be performing essential system updates January 21–25.
Order processing and shipping will pause starting January 21 at 4:00 PM CST and resume on January 26.
Please plan to order in advance for any products needed during this timeframe.
Please contact Customer Service with any questions.
It looks like you are having trouble logging in, please try our dedicated login page.
Grazie per aver verificato il tuo indirizzo email.
C'è stato un errore nella verifica dell'indirizzo email. Riprova o contatta il servizio clienti
Bioluminescenza e Fluorescenza a confronto: guida alla scelta del saggio ideale
12.05.25 – Articolo di Anna Bennett, traduzione di Giacomo Grisafi

Dall'attività enzimatica all'espressione genica, i saggi basati sulla luce sono diventati strumenti fondamentali nella ricerca scientifica. Tra questi, la fluorescenza e la bioluminescenza sono gli approcci più utilizzati per rilevare e quantificare eventi biologici. Entrambi si basano sull'emissione di luce, ma i meccanismi che la generano e le conseguenti implicazioni nella progettazione degli esperimenti sono molto diversi.
Scegliere tra un saggio di fluorescenza e uno di bioluminescenza non è semplice come scegliere tra due reagenti disponibili sullo scaffale. Entrambi hanno qualità e limitazioni a seconda dell'applicazione, della strumentazione e del sistema biologico. In questo articolo blog scopriremo il funzionamento di ciascun metodo, i suoi punti di forza (e di debolezza) e gli elementi da considerare per decidere quale approccio sia più adatto al vostro esperimento.
La fluorescenza si basa su una fonte di luce esterna (solitamente un laser o una lampada ad alta intensità) per eccitare un fluoroforo. Una volta eccitato, il fluoroforo assorbe la luce a una lunghezza d'onda e la emette a una lunghezza maggiore. I filtri vengono poi utilizzati per separare la luce di eccitazione da quella di emissione, consentendo di rilevare il segnale di interesse.
Questo tipo di configurazione richiede una strumentazione complessa; i lettori di fluorescenza o i microscopi devono includere filtri di eccitazione e di emissione, componenti ottici per gestire i percorsi della luce e rivelatori in grado di distinguere tra segnale e rumore di fondo. Questi sistemi offrono flessibilità per il multiplexing e l'imaging, ma i requisiti hardware possono essere costosi e complessi da mettere a punto.
La fluorescenza è molto versatile, anche se la necessità di un'illuminazione esterna pone delle limitazioni. L'autofluorescenza delle cellule, di eventuali composti da testare o dei mezzi di coltura e la dispersione della luce possono interferire con la rilevazione, in particolare quando si lavora con target a bassa espressione o con campioni eterogenei.
La bioluminescenza funziona in modo diverso. Invece di affidarsi a una fonte di luce esterna genera luce attraverso una reazione chimica, tipicamente coinvolgendo un enzima come la luciferasi e un substrato come la luciferina. Quando la luciferasi catalizza l'ossidazione della luciferina, la luce viene prodotta come sottoprodotto della reazione.

Poiché questo processo non richiede luce di eccitazione, i saggi bioluminescenti sono meno suscettibili alle interferenze del background. La maggior parte dei sistemi biologici non emette naturalmente luce bioluminescente, quindi il rapporto segnale-rumore è intrinsecamente elevato. Ciò rende la bioluminescenza particolarmente preziosa per rilevare segnali di bassa intensità in cellule vive o in campioni complessi.
Per quanto riguarda la strumentazione, i saggi bioluminescenti necessitano di un luminometro in grado di rilevare basse emissioni luminose con un'elevata sensibilità. Sebbene questi strumenti non abbiano bisogno della complessità ottica dei sistemi a fluorescenza, la loro sensibilità e la loro gamma dinamica aiutano a ottenere risultati accurati.
Una delle principali differenze tra i saggi di fluorescenza e quelli di bioluminescenza risiede nella loro sensibilità e in particolare nella capacità di ciascun metodo di distinguere il segnale dal rumore di fondo.
I saggi in fluorescenza possono produrre segnali forti, soprattutto con fluorofori luminosi o strategie di rilevazione amplificate. Tuttavia, elevati livelli di fondo possono ridurre la sensibilità effettiva. L'autofluorescenza delle cellule, dei componenti del terreno di coltura o del materiale plastico può interferire con la rilevazione e, con il tempo, il photobleaching riduce l'intensità del segnale, soprattutto negli esperimenti che richiedono diverse acquisizioni nel tempo o effettuati su cellule vive.
Questi fattori rendono più difficile rilevare cambiamenti esigui o bersagli a bassa abbondanza, soprattutto in sistemi biologici complessi in cui è difficile evitare il segnale di fondo.
I saggi bioluminescenti tendono ad avere un rapporto segnale/rumore molto più elevato. Il background è strutturalmente minimo, poiché il segnale è generato enzimaticamente e la maggior parte dei sistemi biologici manca di attività bioluminescente endogena. Ciò rende la bioluminescenza una scelta ideale per quelle applicazioni che hanno nella sensibilità un aspetto fondamentale; come il monitoraggio dell'espressione genica endogena nel tempo o il monitoraggio delle vie di signaling in cellule vive.
Studi recenti lo confermano. Una rassegna del 2023 pubblicata su Biosensors (MDPI) sottolinea i vantaggi dei sistemi bioluminescenti per le applicazioni di biosensori, osservando come la combinazione tra il basso background e l'elevato range dinamico li rendano adatti a rilevare analiti a bassa concentrazione, oltre che per misure cinetiche in tempo reale (1). Allo stesso modo, i biosensori bioluminescenti spesso superano le controparti fluorescenti in ambienti a cellule vive, in particolare quando è necessario distinguere i segnali deboli dal rumore di fondo (2).
Sia la fluorescenza che la bioluminescenza sono ampiamente utilizzate nella ricerca biologica, entrambe più o meno adatte a diversi tipi di esperimenti a seconda dei loro punti di forza. La scelta si riduce spesso a quanto controllo sia necessario sulla risoluzione spaziale, sui tempi dell'esperimento e sulla sensibilità.

I metodi basati sulla fluorescenza sono ben consolidati su un'ampia gamma di applicazioni. La loro capacità di fornire una risoluzione spaziale e temporale li rende ideali per gli esperimenti di imaging, dal tracciamento di proteine marcate in cellule vive alla visualizzazione dell'architettura dei tessuti. Il multiplaxing è un altro punto di forza della fluorescenza; con la giusta combinazione di fluorofori e filtri, i ricercatori possono monitorare più bersagli nello stesso campione.
Queste capacità sono essenziali per applicazioni come la citoflurimetria a flusso e la microscopia a fluorescenza. I progressi nella progettazione di sonde e nella strumentazione, inoltre, continuano ad ampliare le possibilità di questi saggi. Per esempio, l'imaging di cellule vive basato sulla fluorescenza consente ai ricercatori di visualizzare gli eventi cellulari in tempo reale. I contenuti di questa pagina web offrono un dettaglio su come questi strumenti vengono applicati in vari sistemi biologici.
I saggi in bioluminescenza sono perfetti per applicazioni che richiedono un'elevata sensibilità e un interferenza di fondo minima. Poiché il segnale viene generato internamente e non richiede un'illuminazione esterna, la bioluminescenza è una scelta efficace per i saggi a cellule vive e cinetici, soprattutto quando sono coinvolti target a bassa abbondanza.
Gli usi più comuni comprendono il monitoraggio dell'espressione genica, la misurazione delle interazioni proteina-proteina e il monitoraggio di eventi di segnalazione dinamici nel tempo. I saggi bioluminescenti tendono inoltre a essere meno fototossici della fluorescenza. Durante gli esperimenti più lunghi, ciò li rende più delicati per le cellule vive. Se volete approfondire queste applicazioni, su questa pagina web trovate guide approfondite, protocolli e dati di esempio.
L'imaging di cellule vive offre ai ricercatori la possibilità di osservare i processi biologici nel momento esatto in cui avvengono, anziché affidarsi a istantanee fisse o a misurazioni end point. Questo approccio fornisce dati preziosi su eventi cellulari dinamici come l'espressione genica, la localizzazione delle proteine e il signaling cellulare, il tutto preservando l'ambiente cellulare nativo. Se combinato con reporter luminescenti o fluorescenti, l'imaging di cellule vive consente una risoluzione sia spaziale che temporale, rendendo possibile il monitoraggio dei cambiamenti nel tempo e in diversi comparti cellulari.
Per l'imaging, un vantaggio fondamentale della bioluminescenza è l'intrinseca stabilità del segnale bioluminescente, che non richiede un'eccitazione esterna. Ciò consente la visualizzazione diretta della dinamica delle proteine nelle cellule viventi senza la necessità di ripetere l'eccitazione del campione. L'assenza di eccitazione esterna inoltre, riduce anche il rischio di fototossicità e fotobleaching, problemi comuni che possono influire negativamente sulla vitalità delle cellule e sull'integrità del segnale nel tempo.
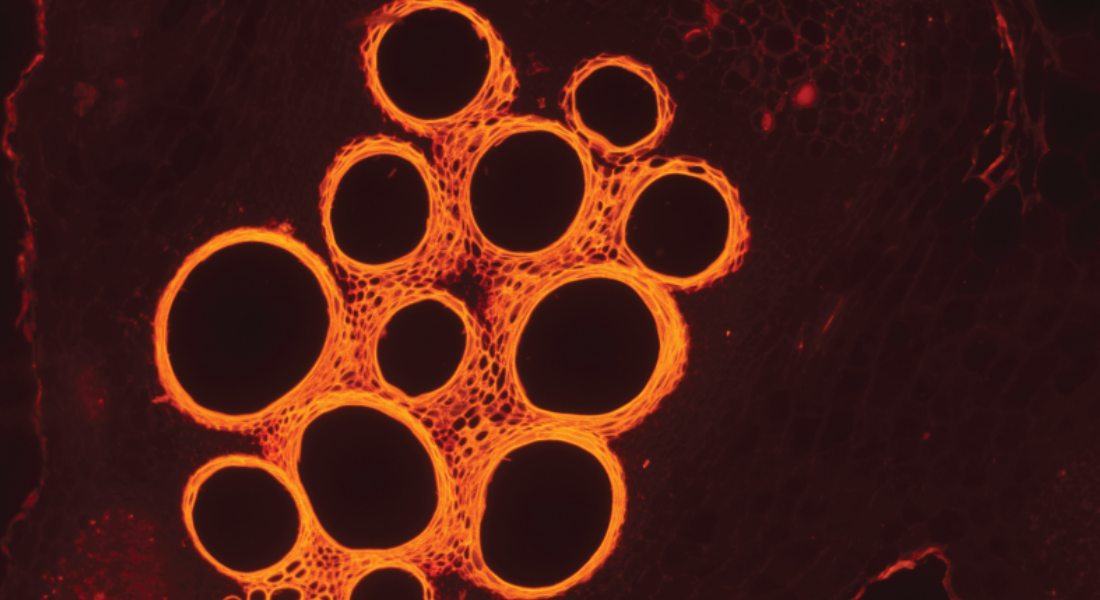
L'imaging su cellule vive offre un approccio sensibile e a basso background per monitorare gli eventi biologici in tempo reale, ideale per le applicazioni in cui la chiarezza del segnale è importante e il minimo disturbo alla cellula può alterare l'esperimento. Strumenti come GloMax® Galaxy Bioluminescence Imager, che integrano luminescenza, fluorescenza e imaging in campo chiaro in un'unica piattaforma supportano un'ampia serie di studi su cellule vive. Tra questi, la visualizzazione delle interazioni proteina-proteina, il monitoraggio della degradazione delle proteine o il target engagement e il monitoraggio delle dinamiche di signling cellulare. Il tutto in sistemi viventi, in cui è importante mantenere inalterate le condizioni fisiologiche.
Per quanto strumenti come GloMax® Galaxy siano in grado di supportare una vasta gamma di applicazioni, la scelta del giusto metodo di rilevamento dipende da diversi fattori, che vanno dall'intensità del segnale fino alla strumentazione. Non esiste un unico strumento quando si parla di saggi basati sulla luce: ogni metodo ha le sue caratteristiche e i suoi punti di forza, e la scelta migliore dipende dalle specifiche esigenze sperimentali.
Se la sensibilità e il basso background sono fondamentali per la vostra ricerca, ad esempio per rilevare segnali deboli in cellule vive o per misurare risposte dinamiche nel tempo, la bioluminescenza è spesso la soluzione migliore. L'assenza di autofluorescenza e di photobleaching la rende particolarmente efficace per i target a bassa abbondanza e per gli studi cinetici a lungo termine.
D'altra parte, la fluorescenza rimane la soluzione ideale per gli esperimenti che richiedono il multiplexing o un'elevata risoluzione spaziale. Applicazioni come la citofluorimetria a flusso e l'imaging tradizionale si affidano spesso alla versatilità e alla potenza visiva delle sonde fluorescenti.
La strumentazione è un altro aspetto da considerare. Per quanto abbiamo già parlato della complessità dei sistemi a fluorescenza rispetto alle esigenze di sensibilità dei lettori di bioluminescenza, vale la pena di notare come anche la compatibilità della piattaforma, i requisiti di produttività e il flusso di lavoro del laboratorio influenzino la decisione finale.
Per confrontare rapidamente le opzioni a disposizione, la seguente tabella evidenzia le caratteristiche principali di ciascun saggio:
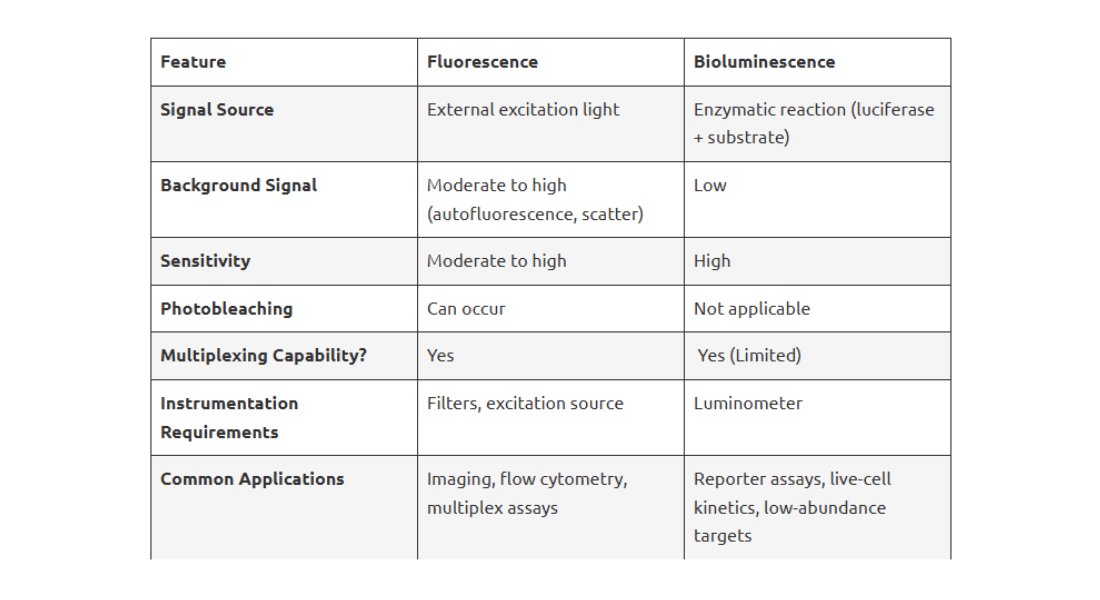
Per concludere, sia la fluorescenza che la bioluminescenza offrono potenti metodi di studio dei sistemi biologici, ma la preferenza per uno o per l'altro dipende dal contesto sperimentale. I saggi a fluorescenza sono adatti alle applicazioni di imaging e multiplexing in cui la risoluzione spaziale gioca un ruolo chiave, mentre i saggi a bioluminescenza si distinguono per la loro sensibilità e la pulizia del segnale, soprattutto negli esperimenti su cellule vive o a bassa abbondanza.
Capire il corretto funzionamento di ogni saggio può aiutare a progettare esperimenti che diano risultati chiari e conclusioni affidabili. Che si tratti di visualizzare le cellule al microscopio o di misurare l'espressione genica in tempo reale, il giusto metodo di rilevamento può fare la differenza.
GloMax® Galaxy è un sistema di imaging in microscopia in grado di visualizzare e raccogliere immagini di altissima qualità da cellule e tessuti che esprimano Nanoluc® o tecnologie da essa derivate come ad esempio NanoBRET®, i sistemi di complementazione NanoBiT®, gli immunoassay della linea Lumit® e il sistema per la quantificazione dell’apoptosi RealTime-Glo™ Annexin V.
Ti è piaciuto questo articolo? Condividilo!